唐山正規外泌體提取試劑廠家直銷
CD47是信號調節蛋白α(SIRPα,也稱為CD172a)的配體,CD47-SIRPα間的結合能夠發出“不要吃我”的信號,從而壓制吞噬作用。病基因RAS能夠促進胰腺病細胞增殖,增強胞飲作用從而促進一些病癥細胞攝取外泌體。合成納米顆粒對細胞有一定毒性作用,但使用外泌體能夠較小化對細胞的毒性。研究人員發現,CD47和病基因KRAS驅動的胞飲作用都會壓制外泌體被循環系統的清理,并增強胰腺病細胞對外泌體的特異性。所以,外泌體的這種特性增強了它們通過遞送RNAi來特異性靶向胰腺病中的KRAS的能力,并且使用外泌體作為單一靶向劑顯著改善了所有實驗PDAC小鼠模型的總生存期。重復離心操作還有可能對囊泡造成損害,從而降低其質量。唐山正規外泌體提取試劑廠家直銷
外泌體與肺病預后:外泌體mirRNA和蛋白質被認為是NSCLC的預后因子。Dejima等在研究NSCLC患者預后的生物標志物時發現,外泌體miR-4257和miR-21的含量顯著上升。此外,還有研究表明,低水平miR-146a-5p的NSCLC患者較高水平miR-146a-5p的NSCLC患者有更高的復發率。Sandfeld-Paulsen等在研究276例NSCLC患者血漿的外泌體時發現,NY-ESO-1是其中對低生存率有顯著影響的標志物。Silva等利用TaqMan低密度芯片的方法系統分析了28位NSCLC患者體內的365種miRNA,其中let-7f、miR-30e-3p和miR-20b表達均下調,進一步研究發現,let-7f和miR-30e-3p水平可以區分早期和晚期NSCLC患者,高水平let-7f和miR-30e-3p與不良預后密切相關。貴陽正規外泌體提取試劑服務電話外泌體提取:高速離心以消除更大的囊泡。

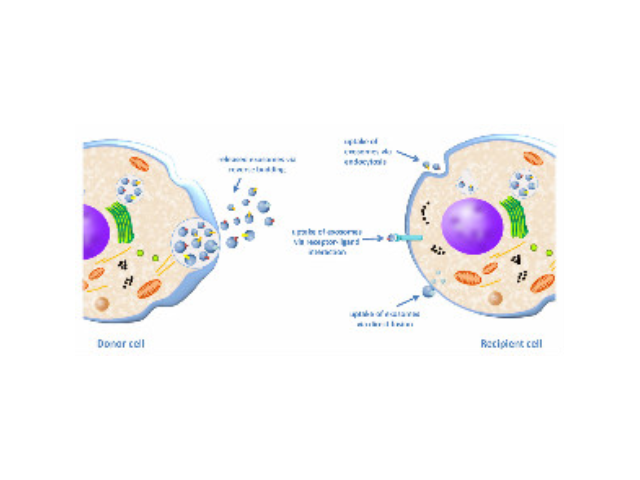
在這項新的研究中,經過基因修飾的外泌體(被稱作iExosome)能夠運送特異性地靶向KRAS突變基因的小RNA分子,從而導致胰腺病模式小鼠病情緩解,增加它們的總存活率。這些研究人員采用了一種被稱作RNA干擾(RNAi)的靶向方法:利用這些天然的納米顆粒(即外泌體)運送小干擾RNA(siRNA)或短發夾RNA(shRNA)分子來靶向胰腺病細胞中的KRAS突變基因,從而影響多種胰腺病模型的一些病癥負荷和存活。他們證實外泌體能夠作為一種高效的RNAi載體發揮作用,這是因為這些納米大小的囊泡(即外泌體)輕松地在體內遷移和進入靶細胞(包括病細胞)中。
具體步驟是:以下所有步驟都在4℃下進行,1、300×g10min,棄沉淀,去除細胞2、2000×g20min,棄沉淀,去除死細胞3、10,000×g30min,棄沉淀,去除細胞碎片等亞細胞成分4、10,000×g70min,棄上清,沉淀即為外泌體5、PBS(每10ml細胞培養液用30mlPBS重懸)清洗沉淀物,混勻,10,000×g70min6、lmlPBS溶解沉淀(外泌體),立即使用或置于-80℃備用。7、一般超速離心法會結合密度梯度離心,這樣得到的外泌體更純,具體做法第4步后蔗糖梯度離心,10,000×g70min,以去除密度大于1.21g/ml的顆粒。優點是:成本低,操作簡單,獲得的囊泡數較多。缺點是:耗時耗力(需用時8-30h,并且每次只能處理6個樣本),獲得的外泌體純度不是很高,高速及重復離心也會對外泌體產生很大的傷害,并且不適用于如血漿和血清等粘性液體生物樣本。外泌體的提取方法:超速離心法(差速離心)。
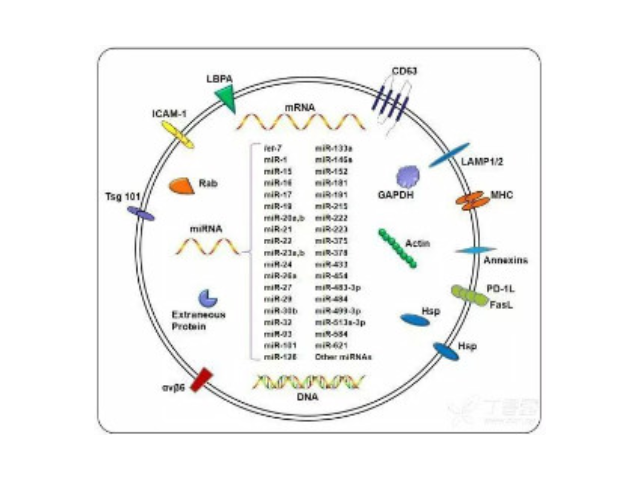
外泌體(exosome),特指直徑在40-100nm的盤狀囊泡。其主要來源于細胞內內溶酶體微粒內陷形成的多囊泡體,經多囊泡體外膜與細胞膜融合后釋放到胞外基質中。現已證實可以分泌外泌體的細胞有:肥大細胞、淋巴細胞、樹突狀細胞、瘤細胞、間充質干細胞等。外泌體在免疫中抗原呈遞、瘤的生長與遷移、組織損傷的修復等生理病理上起著重要的作用。同時,不同細胞分泌的外泌體具有不用的組成成分和功能,可作為疾病診斷的生物標志物。細胞外囊泡是蛋白質、mRNA、miRNA和脂質運輸來完成細胞間通訊通路的重要媒介,根據它們的大小和發生分為三類,包括外泌體、微泡和凋亡小體。現已證實可以分泌外泌體的細胞有:肥大細胞、淋巴細胞、樹突狀細胞、一些病癥細胞、間充質干細胞等。蕪湖正規外泌體提取試劑銷售廠家
對外泌體的研究興趣日益增長,無論是研究其功能還是了解如何將其用于微創診斷的開發。唐山正規外泌體提取試劑廠家直銷
外泌體的提取主要包括以下幾種方式。一是超速離心法,這是目前外泌體提取較常用的方法。此種方法得到的外泌體量多,但是純度不足,電鏡鑒定時發現外泌體聚集成塊,由于微泡和外泌體沒有非常統一的鑒定標準,也有一些研究認為此種方法得到的是微泡不是外泌體。二是過濾離心,這種操作簡單、省時,不影響外泌體的生物活性,但同樣存在純度不足的問題。三是密度梯度離心法,用此種方法分離到的外泌體純度高,但是前期準備工作繁雜,耗時,量少。、唐山正規外泌體提取試劑廠家直銷
- 廈門正規細胞高效轉染試劑銷售廠家 2025-12-19
- 蕪湖正規細胞高效轉染試劑報價 2025-12-19
- 深圳正規鼠尾膠原生產廠家 2025-12-19
- 江蘇如何使用糖原染色試劑盒廠家供應 2025-12-19
- 天津正規糖原染色試劑盒產品介紹 2025-12-19
- 石家莊原代細胞分離試劑盒產品介紹 2025-12-19
- 原代細胞分離試劑盒廠家直銷 2025-12-19
- 深圳細胞高效轉染試劑平均價格 2025-12-19
- 深圳正規細胞高效轉染試劑直銷價 2025-12-19
- 無錫唐山原代細胞分離試劑盒 2025-12-19
- 湖南耐高低溫工程橡膠液壓系統密封 2025-12-19
- 復配實驗室蒸餾水牌子 2025-12-19
- 北京凸輪軸磷化液的優點 2025-12-19
- 浙江敏感肌護膚品好用 2025-12-19
- 杭州中空膠 2025-12-19
- 濰坊柔順劑生產商 2025-12-19
- 江蘇附近門窗幕墻膠供應商 2025-12-19
- 地坪防腐涂料公司哪家好 2025-12-19
- 貴州定型劑銷售廠家 2025-12-19
- 北京工業干膜潤滑劑廠家推薦 2025-12-19