南京紫杉醇
艾沙佐咪不僅在抑制疾病細胞生長方面表現出色,其在實際應用中的效果也備受關注。多項研究顯示,艾沙佐咪能夠明顯抑制多發性骨髓瘤細胞的生長,并在一些小鼠模型中顯示出延長存活期的效果。例如,在異種移植的人漿細胞瘤小鼠模型中,艾沙佐咪明顯抑制了疾病的生長,并延長了小鼠的存活時間。艾沙佐咪處理的小鼠的血液化學特征顯示,其肌酸酐、血紅蛋白和膽紅素的水平均處于正常范圍,這表明艾沙佐咪在抑制疾病細胞的同時,對小鼠的整體健康狀態影響較小。盡管艾沙佐咪在醫治多發性骨髓瘤方面具有明顯療效,但患者在使用過程中仍需注意其可能帶來的副作用,如胃腸道癥狀、血液異常、疲勞等。因此,在使用艾沙佐咪時,患者應在醫生的指導下進行,并定期監測相關指標,以確保醫治的安全性和有效性。新技術為原料藥晶型控制帶來突破。南京紫杉醇
探討卡巴他賽的功能,我們不得不提及它在改善疾病患者生活質量方面的貢獻。盡管疾病醫治常常伴隨著一系列副作用,但卡巴他賽在延長生存期的同時,也努力減輕患者的癥狀負擔。它通過精確靶向疾病細胞,減少對正常細胞的傷害,從而降低了傳統化療常見的毒副反應,如骨髓抑制、神經毒性等。卡巴他賽的研發和應用還推動了個性化醫療的發展,醫生可以根據患者的基因型和疾病特征,制定更加精確的醫治方案。這不僅提高了醫治的成功率,也體現了現代醫學從一刀切向量體裁衣轉變的趨勢。隨著對卡巴他賽作用機制的深入研究,未來有望開發出更多基于其原理的新型抗疾病藥物,為疾病患者帶來更多福音。南京紫杉醇發酵原料藥的菌種選育技術關鍵。
Ixazomib citrate能抑制細胞的侵襲能力,降低MMP2/9的表達和分泌水平,從而展現出抗疾病的潛力。這些功能使得Ixazomib citrate在疾病醫治領域具有廣闊的應用前景,特別是在多發性骨髓瘤等血液疾病的醫治中。在體內實驗中,Ixazomib citrate也表現出了明顯的抗疾病活性。例如,在人漿細胞瘤MM.1S異種移植小鼠模型中,Ixazomib citrate能夠明顯抑制疾病生長并延長小鼠的存活期。同時,醫治小鼠的血液化學特征顯示肌酐、血紅蛋白和膽紅素水平正常,這表明Ixazomib citrate具有較好的安全性和耐受性。這些實驗結果不僅進一步驗證了Ixazomib citrate的抗疾病效果,也為其在臨床上的應用提供了有力的支持。
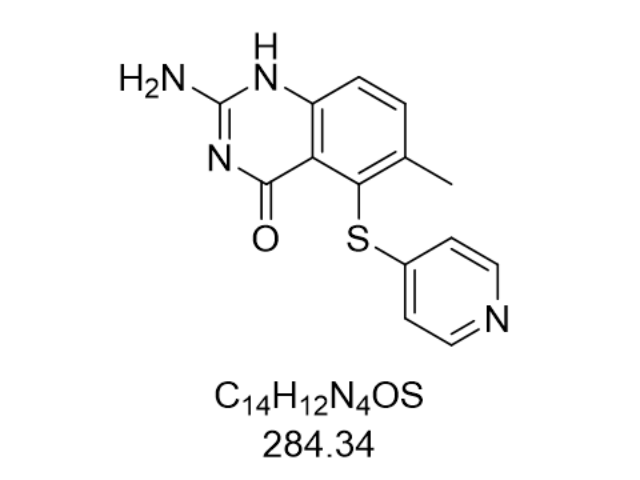
諾拉曲特(Nolatrexed,CAS:147149-76-6)作為胸苷酸合成酶抑制劑,其重要性能源于對靶點酶的精確作用機制。胸苷酸合成酶是DNA復制過程中催化脫氧尿苷酸(dUMP)轉化為脫氧胸苷酸(dTMP)的關鍵酶,而諾拉曲特通過模擬天然底物結構,以高親和力占據酶的活性中心。其分子設計基于胸苷酸合成酶的三維晶體結構,采用計算機輔助藥物設計技術優化喹唑啉骨架,使藥物分子能夠同時結合酶的兩個葉酸結合位點,形成穩定的復合物。這種雙重結合模式不僅增強了抑制效力,還通過空間位阻效應阻止底物進入,從而徹底阻斷dTMP的合成。實驗數據顯示,諾拉曲特在體外對肝疾病細胞系的IC50值低至0.1-0.5μM,明顯低于傳統抗代謝藥物5-氟尿嘧啶(5-FU)的2-5μM范圍,表明其具有更強的細胞毒性。體內研究進一步證實,在裸鼠肝疾病移植瘤模型中,諾拉曲特以50mg/kg劑量連續給藥14天,可使疾病體積縮小65%,而同等劑量5-FU只抑制38%,凸顯其作為新一代抗疾病藥物的潛力。原料藥作為制劑重要成分,其質量直接影響藥品療效與患者用藥安全。
臨床應用中,紫杉醇的劑型創新明顯提升了療效與安全性。傳統紫杉醇注射液因含聚氧乙烯蓖麻油(Cremophor EL)表面活性劑,易引發嚴重過敏反應(發生率約40%),需在使用前進行、苯海拉明和西咪替丁的三聯預處理。2005年上市的紫杉醇脂質體通過將藥物包裹于磷脂雙分子層中,降低了過敏風險(發生率降至2%),但制劑穩定性受pH值影響較大。2010年問世的白蛋白結合型紫杉醇(nab-Paclitaxel)則利用人血清白蛋白的自然轉運特性,通過gp60受體介導的內皮細胞跨膜轉運,使疾病組織藥物濃度提高3.3倍,單藥劑量可從傳統制劑的175mg/m2提升至260mg/m2,且無需預處理。臨床研究顯示,在轉移性乳腺疾病醫治中,nab-Paclitaxel組客觀緩解率達48%,明顯高于傳統制劑的26%。此外,針對耐藥問題開發的紫杉醇聚合物膠束,通過PEG-PLGA嵌段共聚物形成納米顆粒,將藥物包裹于疏水重要,實現了EPR效應(增強滲透與滯留效應)下的靶向遞送,使疾病組織藥物蓄積量提高5.8倍。原料藥合成路線設計追求高效環保。杭州沙庫比曲纈沙坦鈉
原料藥的生產工藝需不斷改進,以適應新的法規要求。南京紫杉醇
在研發與市場層面,Avibactam鈉經歷了從實驗室發現到臨床轉化的漫長歷程。該分子較早由Hoechst Marion Roussel(現賽諾菲)的化學家于20世紀90年代中期合成,后經Novexel公司開發,與Forest Laboratories(現Allergan)合作推進臨床研究。2015年,FDA批準頭孢他啶/阿維巴坦用于醫治cIAI和HAP/VAP,2016年獲得EMA批準,商品名為Avycaz?(美國)和Zavicefta?(歐洲)。2019年,輝瑞通過收購阿斯利康小分子業務獲得全球研發權(北美除外)。中國市場方面,該組合于2009年獲NMPA批準,2021年齊魯制藥首仿上市,推動院內銷售額快速增長(2022年達4.63億元)。原料藥領域,全球登記企業達10家(中國8家),2022年用量突破2221kg,反映市場需求激增。南京紫杉醇
- 5-氨基乙酰丙酸甲酯鹽酸鹽咨詢 2025-12-20
- N-(2-(二乙基氨基)乙基)-2 2025-12-20
- 2-溴-4-氯苯胺批發 2025-12-20
- 1-溴-2-芐氧基乙烷報價 2025-12-20
- 銀川反-2-己烯醛 2025-12-20
- 拉薩二氫(神經)鞘氨醇 2025-12-20
- 上海5-氨基乙酰丙酸甲酯鹽酸鹽 2025-12-20
- 二苯甲醚基碘化碘鎓鹽現貨 2025-12-20
- 南京五氟本肼 2025-12-20
- 5-氟吲哚-2-酮生產廠家 2025-12-19
- 青海植物冠層光合氣體交換測量系統一體化 2025-12-20
- 洛龍附近醫護型養老護理院一個月多少錢 2025-12-20
- 2-溴-4-氯苯胺批發 2025-12-20
- 江西IEC62133電池模組 2025-12-20
- 上海黍峰生物多功能群體光合儀多少錢 2025-12-20
- 西工附近有臨終關懷服務的醫療型養老中心 2025-12-20
- 浙江常用哺光儀 2025-12-20
- 山西聚甲醛產品 2025-12-20
- 醫療器械結扎夾掛網 2025-12-20
- 山西國內助膝器運動人群 2025-12-20