地拉羅司廠家供應
安全性管理方面,多西他賽的劑量限制性毒性呈現特征性表現。中性粒細胞減少癥發生率達89%,其中Ⅲ/Ⅳ級占76%,但通過G-CSF支持可使嚴重被染率控制在5%以下。過敏反應雖發生率約26%,但通過8mg bid預處理3天方案,嚴重過敏反應(支氣管痙攣、低血壓)發生率已降至0.7%。體液潴留作為另一重要不良反應,在累積劑量達400mg/m2時發生率升至65%,表現為下肢水腫、胸腔積液甚至心包積液,但停藥后3個月內可完全消退。神經毒性方面,23%的患者出現感覺神經異常,但多為Ⅰ-Ⅱ級,只3%需要劑量調整。藥物相互作用管理中,除需規避CYP3A4抑制劑外,與順鉑聯用時建議先給予多西他賽,可避免順鉑導致的腎去除率下降;而與蒽環類藥物序貫使用時,則需先給予蒽環類以防止心臟毒性疊加。這些安全性特征的明確,為制定個體化劑量調整方案(如從75mg/m2減量至60mg/m2)提供了科學依據,使醫治中斷率從初始方案的21%降至優化后的9%。原料藥的生產過程優化需考慮成本、效率和質量平衡。地拉羅司廠家供應
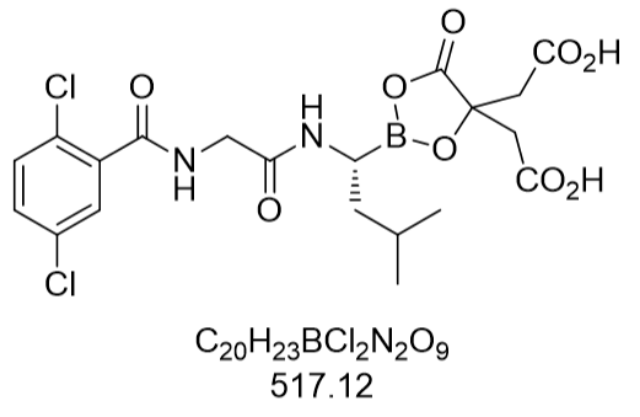
原料藥的純度直接決定藥品的安全性與有效性,是質量控制的重要環節。原料藥中的雜質可能來源于合成工藝的副反應、殘留溶劑、重金屬或降解產物,這些雜質若未被有效控制,可能引發毒性反應或降低藥效。例如,基因毒性雜質即使含量極低,也可能導致DNA損傷,因此需采用高靈敏度的分析方法(如LC-MS)進行檢測。殘留溶劑的控制同樣嚴格,國際人用藥品注冊技術協調會(ICH)對不同溶劑的限量有明確規定,如一類溶劑(如苯)因致疾病性被完全禁止使用。原料藥的純度提升依賴于合成工藝的優化與精制技術的改進,如重結晶、色譜分離或膜過濾等。此外,原料藥的粒度分布也會影響制劑的均勻性與穩定性,細粉可能導致含量不均,而粗粉則可能影響溶解速率。因此,純度控制需貫穿原料藥生產的全過程,從原料檢驗、中間體控制到成品放行,每一環節均需嚴格遵循質量標準。長沙美法侖原料藥進出口需符合兩國藥監部門法規,辦理通關審批手續。
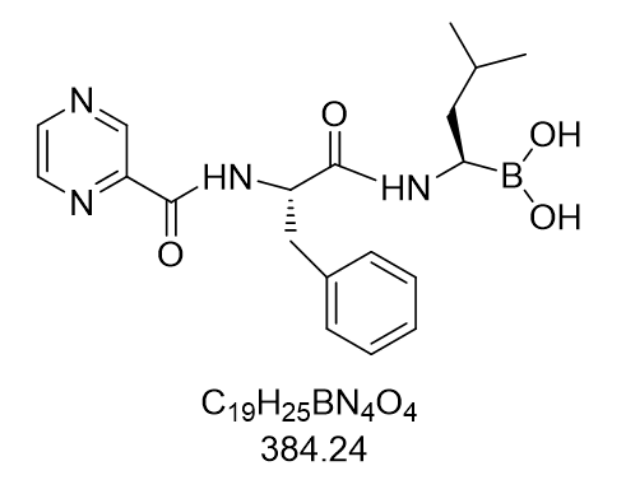
從分子結構到臨床實踐,硼替佐米的設計體現了精確醫療的重要理念。其化學名為N-(2-吡嗪羰基)-L-苯丙氨酸-L-亮氨酸硼酸,分子式C19H25BN4O4,通過模擬肽鏈結構與蛋白酶體活性位點形成共價鍵,這種鎖鑰式結合模式使其對疾病細胞的殺傷效率較傳統化療藥物提升3倍以上。在多發性骨髓瘤模型中,硼替佐米可誘導骨髓瘤細胞表面CD38抗原表達上調,為后續聯合達雷木單抗(CD38單抗)醫治提供理論依據。2012年發表的《新英格蘭醫學雜志》研究顯示,硼替佐米聯合來那度胺和的三藥的方案,使新診斷MM患者的5年生存率從55%提升至78%,徹底改變了該領域醫治即緩解,緩解即復發的惡性循環。值得注意的是,其藥代動力學特性亦支持個性化給藥:健康志愿者單次給藥后,血漿濃度呈雙相衰減,終末半衰期為9-15小時,而疾病患者因蛋白酶體表達上調,藥物去除率降低30%,提示需根據患者代謝特征調整劑量。這種從分子機制到臨床方案的深度解析,使硼替佐米成為疾病靶向醫治中基礎研究-轉化醫學-臨床應用閉環的典范。
德蘭佐米(Delanzomib,CAS號847499-27-8)作為蛋白酶體抑制劑家族的一員,其研發歷程凝聚了眾多科學家的智慧與心血。從開始的分子設計到后期的臨床試驗,每一步都充滿了挑戰與突破。該藥物的合成工藝復雜精細,需要嚴格控制反應條件和純化步驟,以確保產品的質量和穩定性。在藥物代謝動力學方面,德蘭佐米展現出良好的吸收、分布和排泄特性,使其在體內能夠維持有效的血藥濃度,從而達到很好的醫治效果。同時,針對德蘭佐米可能產生的不良反應,研究人員也進行了詳盡的評估,并制定了相應的預防和應對措施,以保障患者的安全。未來,隨著對德蘭佐米作用機制的進一步解析和臨床應用的不斷拓展,我們有理由相信,這一創新藥物將在疾病醫治中發揮更加重要的作用。原料藥企業加強產學研合作促發展。
在醫治晚期或轉移性GIST患者中,蘇尼替尼也展現出了明顯的療效,通過抑制KIT和PDGFR等靶點,有效阻斷了疾病細胞的生長信號,減少了新血管生成,進而抑制了GIST的進展。蘇尼替尼的這些功效使其成為了疾病醫治中不可或缺的藥物之一,為無數患者帶來了新的醫治希望。蘇尼替尼也展現出了在醫治其他類型疾病中的潛力。例如,在神經內分泌瘤和肝細胞疾病的醫治中,蘇尼替尼通過靶向抑制特定的受體,如VEGFR、PDGFR和RET等,抑制了血管生成和疾病細胞的增殖,從而減少了疾病的生長。這些研究成果進一步拓寬了蘇尼替尼的臨床應用范圍,為其在更多類型疾病的醫治中提供了可能。盡管蘇尼替尼在使用過程中可能會出現一些副作用,但在醫生的指導下進行個體化的醫治,并密切監測患者的藥物反應,可以較大限度地發揮其療效,同時確保患者的安全。原料藥生產過程中的中間產品需嚴格檢驗,合格后方可流轉。長春硼替佐米
特色原料藥對應技術到期制劑,技術壁壘高,附加值可達大宗品種3倍。地拉羅司廠家供應
艾沙佐咪(Ixazomib citrate,CAS:1239908-20-3)作為第二代口服蛋白酶體抑制劑,其重要性能體現在對20S蛋白酶體β5亞基的高效抑制作用上。該藥物通過可逆性結合胰凝乳蛋白酶樣蛋白水解位點(β5),以3.4 nM的IC50值和0.93 nM的Ki值實現精確阻斷,明顯優于第1代抑制劑硼替佐米(IC50約13 nM)。臨床前研究顯示,Ixazomib對β1(類caspase樣)和β2(類胰蛋白酶樣)亞基的抑制作用較弱(IC50分別為31 nM和3500 nM),這種選擇性抑制特性使其在保持抗疾病活性的同時,減少了對正常細胞蛋白酶體功能的干擾。在多發性骨髓瘤細胞系H929和MM.1S的體外實驗中,藥物處理導致泛素化蛋白明顯積累,并誘導PARP裂解(細胞凋亡標志物),證明其通過阻斷蛋白酶體介導的蛋白質降解通路,觸發疾病細胞內源性凋亡程序。此外,動物模型研究顯示,Ixazomib在不影響小鼠體重和部位功能的前提下,可明顯抑制漿細胞瘤生長,疾病復發率較硼替佐米醫治組降低42%,這與其更持久的靶點抑制作用直接相關。地拉羅司廠家供應
- 5-氟吲哚-2-酮生產廠家 2025-12-19
- 黑龍江7-氟-2-吲哚酮 2025-12-19
- 3-丁烯-1-醇3-Buten-1-ol售價 2025-12-19
- 2-碘-5-溴嘧啶求購 2025-12-19
- 2-氧化吲哚-6-甲酸甲酯采購 2025-12-19
- 河北5-氟-2-甲氧基-3-吡啶甲醛 2025-12-19
- 蘭州對甲氧基苯乙胺 2025-12-19
- 2 2025-12-19
- 合肥1-溴-2-芐氧基乙烷 2025-12-19
- N-Boc-4-哌啶酮-3-甲酸甲酯生產 2025-12-18
- 松江區定制吻合器工廠直銷 2025-12-19
- 深圳醫院智慧管理系統多少錢一套 2025-12-19
- 山西疫苗佐劑QS-21 2025-12-19
- 姑蘇區常見一次性注射器資費 2025-12-19
- 武漢本地活細胞成像分析系統直銷價格 2025-12-19
- 銀杏葉片工廠 2025-12-19
- 珠海有實力的nmn定制廠家 2025-12-19
- 冠層光合速率多通道冠層光合儀廠家推薦 2025-12-19
- 中科院群體光合儀多少錢 2025-12-19
- 10mm結扎夾產品圖片 2025-12-19