上海貨號高鹽核酸酶用途
ArcticZymes Technologies致力于提供高質量產品,具有良好的批間一致性、穩定可靠的質量、及時的文件及技術支持。ArcticZymes所有產品的開發、生產及銷售等都符合ISO13485:2016質量管理體系標準;鑒于生物制品更嚴格的質控要求,廠家對鹽活性核酸酶系列產品(Salt Active Nucleases,SANs)的生產及質控,在符合ISO13485:2016體系基礎上,增加了cGMP相應要求,如生產用原輔料是Non-animal和Non-plant來源的,終產品經過0.22μm過濾sterilization,放行檢測包括microbes、fungus及內毒檢測等,所有標準符合USP-EP要求。SAN HQ高鹽核酸酶是用Pichia pastoris表達的重組非特異性內切核酸酶。上海貨號高鹽核酸酶用途
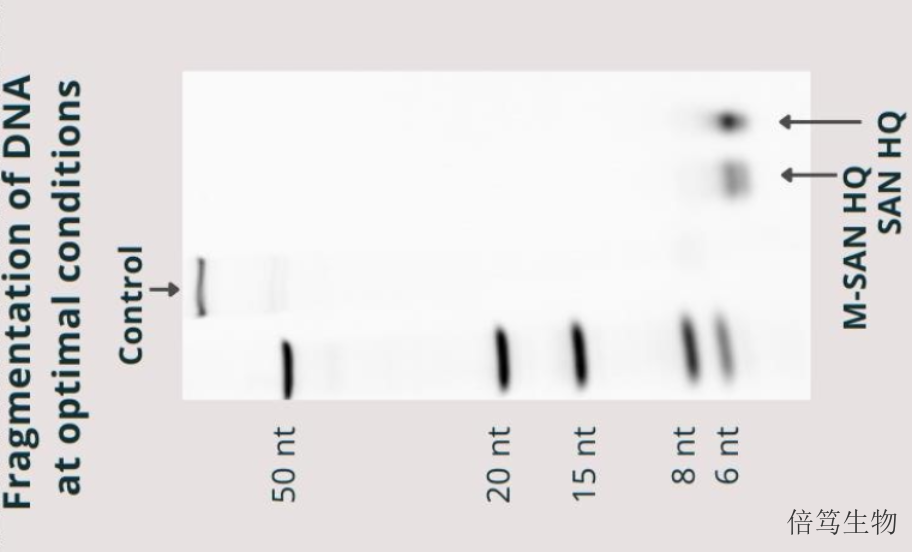
宿主細胞DNA(HCD)殘留以染色質形式存在,其中有帶負電荷的DNA、帶正電荷及疏水區段的組蛋白,就像膠帶一樣能夠吸附很多物質,包括各種雜蛋白、色譜填料、目的病毒顆粒。非特異吸附雜蛋白,會影響蛋白雜質(如HCP)等的去除;吸附到色譜填料上,會降低色譜分離純化效率;吸附到目的病毒顆粒時,會影響目的產物的穩定性,從而降低目的產物的得率。因此,從生產工藝層面來講,一定要去除HCD,從而能夠簡化工藝、提高目的產物的產量。 江西質量高鹽核酸酶量大優惠黃山高鹽核酸酶服務哪家好呢,歡迎咨詢上海倍篤生物 。
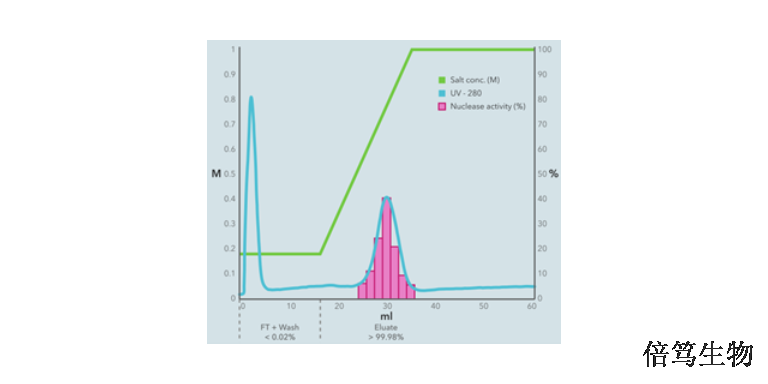
從國內來看,由于 AAV 基因藥物研發管線絕大部分集中在眼科遺傳病上,載體用量較小,三質粒共轉染 AAV 系統足以滿足未來的臨床及商業需求,因此,國內的 AAV 生產系統主要以三質粒為主。然而,考慮到未來 AAV 基因藥物在血液、神經系統、肌肉系統等領域的臨床應用,三質粒系統顯然難以勝任。如藥明生基從國外收購了 OXGENE 的輔助腺病毒 AAV 生產系統 TESSA,據報道較三質粒系統有10倍的提升;而基因藥物 CDMO 企業北京五加和基因則在國內率先采用了陳海峰博士的威洛克公司授權的Bac-to-AAV 系統,憑借公司在病毒載體領域持續30年的研發經驗,不斷摸索、試驗,終于在臨床級生產方面獲得了巨大的成功,為 AAV 基因藥物管線研發公司錦籃基因進行多批次臨床 CDMO 代工生產。
在抗體藥物及核酸藥物領域,倍篤生物產品線涵蓋藥物研發的全流程,主要用——RNA轉染試劑、生物活性物質純化分離用填料產品、ADC的payload抗體(如anti-DXD、anti-Eribulin、anti-MMAE等)、動物造模用陽性及陰性抗體、泊洛沙姆P 188 Bio、工藝雜質及外源污染物殘留檢測產品、抗體結構域分析蛋白酶、蛋白聚糖分析水解酶等,品牌有德國Genovis、德國BASF、中國君研生物、中國金傳生物、中國毫厘科技、中國再帆生物等。這些國產品牌都具有國內自研、自產能力,批次生產穩定可靠、品質可控,為行業發展提供更多國產選擇。SAN HQ高鹽核酸酶在高鹽濃度下活性更適,DNA去除效率更高。

宿主細胞DNA殘留的擔憂是基于致ai風險理論,特別是生產細胞系所包含的致ai序列,比如較常見腺病毒基因E1A和E1B(HEK293, PerC.6 和CAP 細胞系),人乳tou瘤病毒E6和E7基因(HeLa細胞系)等。當使用致ai細胞系生產AAV時,下游純化須盡可能減少殘留DNA。工業上一般使用核酸酶分解殘留DNA,普遍認為小于200 bp的DNA片段可有效降低致ai風險。宿主細胞蛋白殘留與免疫原性、炎癥或過敏性休克有關。盡管與非人類的生產原料相比(非人類細胞系如BHK21或昆蟲細胞,以及輔助病毒如HSV、腺病毒、桿狀病毒),人類細胞免疫原性比較弱。GMP級別SAN HQ提供了更多的監管保證。在線高鹽核酸酶用途
US FDA指南要求:重組生物制品終產品中,核酸雜質含量低于10ng/dose。上海貨號高鹽核酸酶用途
細胞基因藥物的基因遞送有病毒及非病毒兩種方式,其中病毒遞送更為常用。在病毒遞送路徑中,腺相關病毒(AAV)和慢病毒(Lentivirus)是常用的兩種載體;差別是病毒基因組的存在形式,AAV的基因組一般不整合到染色體中,以游離形式存在于染色體之外,且一般會表達數年之久;而慢病毒的基因組則會整合到染色體達到長期持續表達的目的。此外,其它用于基因藥物的病毒載體有單純皰疹病毒(HSV)、痘苗病毒(Vaccina Virus)、痘病毒(Poxviruses)。上海貨號高鹽核酸酶用途
- 70950-202高鹽核酸酶價格表 2025-12-19
- 宣城SAN HQ高鹽核酸酶報價表 2025-12-19
- 上海貨號高鹽核酸酶廠家直銷 2025-12-19
- 重慶貨號高鹽核酸酶銷售電話 2025-12-19
- 安徽70950-202高鹽核酸酶 2025-12-19
- 天津哪里有高鹽核酸酶哪家公司銷售 2025-12-19
- 北京綜合高鹽核酸酶用途 2025-12-19
- 歷城區倍篤高鹽核酸酶供應商 2025-12-19
- 連云港70921-160高鹽核酸酶銷售電話 2025-12-19
- 市中區倍篤高鹽核酸酶工廠直銷 2025-12-19
- 佛山1470nm國產半導體激光治療儀廠家電話 2025-12-19
- 吳江區服務軟霧吸入器加盟連鎖店 2025-12-19
- 松江區定制吻合器工廠直銷 2025-12-19
- 深圳醫院智慧管理系統多少錢一套 2025-12-19
- 山西疫苗佐劑QS-21 2025-12-19
- 姑蘇區常見一次性注射器資費 2025-12-19
- 武漢本地活細胞成像分析系統直銷價格 2025-12-19
- 附近哪里有助腿器誠信合作 2025-12-19
- 銀杏葉片工廠 2025-12-19
- 珠海有實力的nmn定制廠家 2025-12-19