廣西免疫組化全景掃描性價比
0. 發育生物學利用全景掃描技術追蹤生物體從受精卵到成體的發育全過程,通過定時成像系統每隔數分鐘記錄一次細胞分裂、分化的動態變化,能構建***形成的三維全景模型,清晰展示心臟、肝臟等***從細胞團到功能***的形態建成過程。結合基因芯片檢測的基因表達時序變化,可揭示發育過程中基因表達調控與形態建成的關聯,比如在斑馬魚胚胎發育研究中,發現了特定基因的時空表達模式與體節形成的精確對應關系,深化了對生命發育機制的認識,為先天性疾病的病因研究提供了重要線索。全景掃描觀察種子萌發,記錄胚根突破種皮及子葉展開的實時狀態。廣西免疫組化全景掃描性價比

在再生生物學研究中,全景掃描技術實現了對生物體損傷修復過程的動態、多尺度觀測。通過高分辨率***成像和三維重構技術,研究者能夠精確追蹤再生過程中細胞的遷移路徑(如干細胞向損傷位點的定向募集)、增殖熱點(如芽基組織的形成)以及分化軌跡(如軟骨、肌肉和神經的同步再生)。以蠑螈肢體再生為例,全景掃描結合熒光標記技術清晰呈現了損傷后24小時內表皮細胞的快速覆蓋、72小時后多能干細胞的聚集,以及后續的空間有序分化——外層形成軟骨模板,內部肌纖維再生,同時伴隨血管和神經的精細延伸。結合單細胞轉錄組測序,研究發現FGF10、BMP2等基因在再生不同階段呈現動態表達,調控細胞命運決定。此外,全景掃描還揭示了細胞外基質(ECM)重塑對再生微環境的關鍵作用,如膠原纖維的定向排列引導組織形態發生。這些發現為人類再生醫學提供了重要啟示,例如通過模擬蠑螈的ECM動態變化,可優化生物支架材料的設計,促進慢性傷口愈合;而干細胞時空***策略則可能應用于***體外再生,減少移植排斥風險。未來,結合人工智能動態建模,全景掃描技術有望在再生醫學領域實現更精細的調控,推動創傷修復和退行性疾病***的發展。江蘇髓鞘全景掃描銷售電話全景掃描觀察免疫突觸形成,展示 T 細胞與抗原呈遞細胞的相互作用。
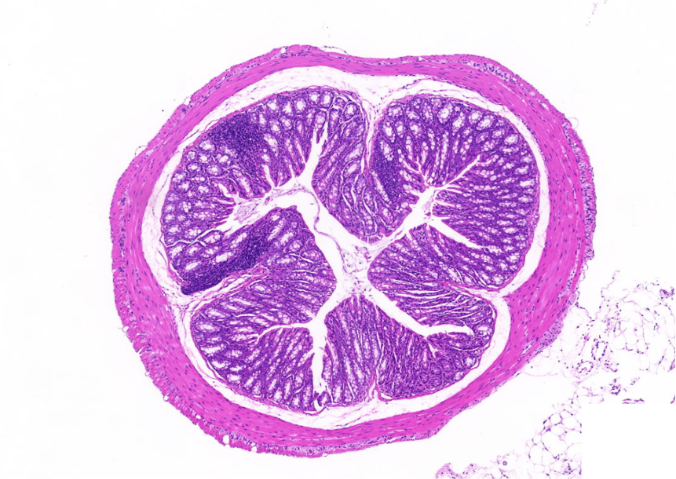
0. 分子生物學研究中,全景掃描技術可結合熒光原位雜交與超高分辨率成像,對細胞內的 DNA、RNA 分子進行全域定位與動態追蹤,清晰呈現染色體的空間結構、基因的表達位置及 RNA 的轉運路徑。通過分析這些分子的空間排布與相互作用,揭示基因調控網絡的時空動態,例如在研究基因表達調控時,全景掃描發現了特定轉錄因子與基因啟動子的結合位置及結合強度隨細胞周期的變化,為理解基因表達的精確調控機制提供了直接證據,也為基因編輯技術的優化提供了參考。
在噬菌體研究中,全景掃描技術 通過超高時空分辨率成像系統,實現了對 噬菌體-細菌互作 全過程的動態可視化。該技術整合 冷凍電鏡單顆粒分析(分辨率達2.8?)、高速原子力顯微鏡(HS-AFM,毫秒級動態捕捉)和 熒光標記示蹤,可解析從 初始吸附 到 裂解釋放 的分子細節:侵染起始階段冷凍電鏡全景重構 顯示T4噬菌體尾絲蛋白gp37通過 三聚體前列結構域(殘基Asp1021-Glu1098)特異性識別大腸桿菌OmpC孔蛋白的 表面環狀區(L3 loop)高速AFM動態掃描 發現噬菌體λ的J蛋白在10秒內完成 宿主Lamb受體的多點錨定(結合力≥50pN)基因組注入機制熒光量子點標記 的全景追蹤顯示,T7噬菌體DNA以 5kb/秒的速度 通過收縮的尾鞘注入細胞,伴隨宿主 質子動力勢(Δψ)的瞬時崩潰同步輻射X射線成像 捕獲到噬菌體Φ29的 portal蛋白旋轉(每秒120轉),驅動DNA穿越細胞膜抗性突破策略超分辨顯微鏡(STORM)發現,CRISPR-Cas9抗性菌株的 胞內噬菌體衣殼 會*** SOS響應系統,通過RecA蛋白介導的 原噬菌體*** 逃逸切割全景掃描觀察骨髓造血,呈現造血干細胞分化為各類血細胞的過程。
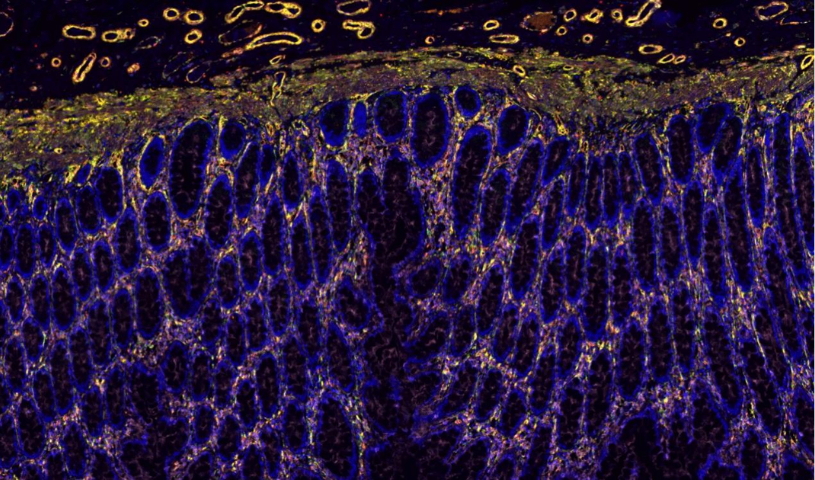
0. 免疫學研究中,全景掃描技術可對免疫***如淋巴結、脾臟進行全域成像,清晰呈現 T 細胞、B 細胞、巨噬細胞等免疫細胞的空間分布及相互作用。通過標記不同免疫細胞表面的特異性分子,結合實時成像,能追蹤免疫細胞在抗原刺激后的活化、增殖及遷移軌跡,揭示免疫應答的啟動與調控機制。例如在研究自身免疫性疾病時,全景掃描發現了免疫細胞異常聚集與組織損傷的關聯模式,為疾病的免疫調節***提供了新的靶點和策略,同時也助力疫苗免疫效果的評估,通過觀察免疫細胞的活化程度判斷疫苗的有效性。利用全景掃描研究白蟻巢穴,揭示其復雜通道結構與通風的關系。江蘇髓鞘全景掃描銷售電話
全景掃描評估植物疫苗效果,檢測葉片內抗體的合成與分布情況。廣西免疫組化全景掃描性價比
細胞自噬研究中,全景掃描技術的應用極大地推動了該領域的動態監測能力。通過高分辨率熒光標記技術,研究人員能夠實時追蹤自噬相關蛋白(如LC3、p62等)的時空分布,精確記錄自噬體從起始、擴展、成熟到與溶酶體融合的全過程。結合高速成像和三維重構技術,可量化分析自噬體在細胞內的運動速率、軌跡特征及數量波動。蛋白質組學數據的整合進一步揭示了關鍵調控節點:在營養缺乏時,mTOR信號通路抑制誘導自噬***;氧化應激條件下,AMPK和FOXO通路調控自噬體形成。值得注意的是,在**微環境中,全景掃描發現自噬體在*細胞的核周區域異常聚集,這種空間分布紊亂與溶酶體酸化障礙相關,導致化療藥物無法被有效降解而形成耐藥性。基于這些發現,研究者已開發出靶向自噬體-溶酶體融合環節的抑制劑(如羥氯喹),并在臨床試驗中驗證其可增強傳統化療效果。這些成果不僅為*****提供了新策略,更完善了對自噬在細胞代謝重編程、受損細胞器***等穩態維持機制中的系統性認知。廣西免疫組化全景掃描性價比
- 浙江國產科研一抗怎么樣 2025-12-19
- 新疆小鼠科研一抗一般多少錢 2025-12-18
- 湖北心臟病理切片24小時服務 2025-12-18
- 廣西免疫組化全景掃描性價比 2025-12-18
- 甘肅髓鞘全景掃描性價比 2025-12-18
- 遼寧免疫組化全景掃描單價 2025-12-18
- 四川科研一抗市場價格 2025-12-18
- 湖北犬科研一抗咨詢報價 2025-12-17
- Masson全景掃描電話多少 2025-12-17
- 廣東病理切片實驗效果 2025-12-16
- 金山區便宜的吻合器費用 2025-12-19
- 專科醫院信息系統報價 2025-12-19
- 微藻提取藻油EPA原料售后服務有哪些 2025-12-19
- 上海名優內窺鏡市價 2025-12-19
- 湖南無菌肛腸外科套扎器供應商 2025-12-19
- 黃浦區本地鼻氧管價錢 2025-12-19
- 本地定制式助聽器上門驗配 2025-12-19
- 上海高效熱原檢測MAT試劑盒 2025-12-19
- 楊浦區名優鼻氧管電話多少 2025-12-19
- 湖南聚醚醚酮銷售廠家 2025-12-19