揚州70950-150中鹽核酸酶采購
大規(guī)模生產(chǎn)階段,AAV/LV載體生產(chǎn)流程跟抗體、疫苗類藥物的生產(chǎn)類似,主要包含上游培養(yǎng)、下游純化及制劑部分。上游培養(yǎng)分為質(zhì)粒開發(fā)、細胞擴增、三質(zhì)粒共轉(zhuǎn)染及病毒載體生產(chǎn)等步驟。下游純化分為細胞裂解釋放AAV病毒顆粒(可以通過去污劑、機械作用、高滲或凍融操作等)or收獲細胞上清液得到含LV病毒原液、加入核酸酶以減少宿主細胞核酸污染、澄清是通過離心或過濾等方法去除細胞碎片和雜質(zhì)等、超濾濃縮以減少后續(xù)色譜純化體系、親合及離子交換等純化得到高純度病毒載體。制劑部分主要是超濾更換緩沖液、過濾除菌及制劑灌裝等。中鹽核酸酶適宜pH范圍廣(pH7.2-8.7),且在125–250mM鹽濃度內(nèi)具有較高活性。揚州70950-150中鹽核酸酶采購
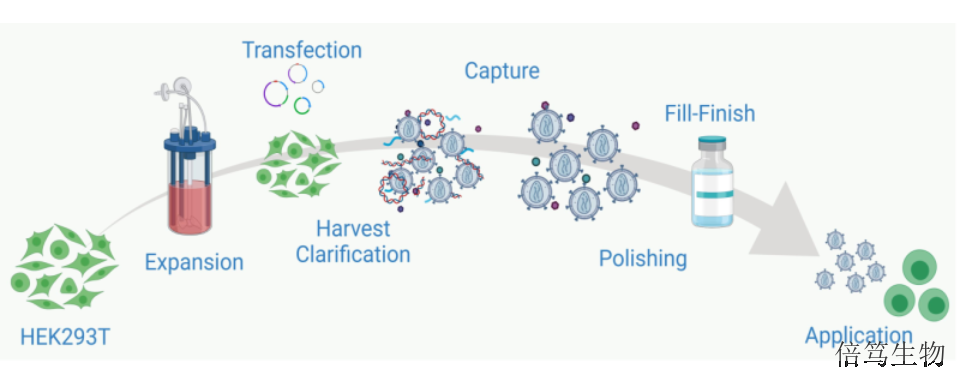
這款核酸酶的適宜pH范圍很廣(pH 7.2 - 8.7),且在125 – 250 mM鹽濃度內(nèi)具有優(yōu)活性。在細胞培養(yǎng)液或收獲的培養(yǎng)上清中,不需調(diào)整任何組分,直接加入M-SAN HQ即可表現(xiàn)良好核酸酶活性。相比傳統(tǒng)的全能核酸酶,M-SAN HQ中鹽核酸酶在生理鹽條件下,對HCD的去除更高效、更徹底。因此,M-SAN HQ中鹽核酸酶非常適合部分病毒載體(如慢病毒、逆轉(zhuǎn)錄病毒及溶瘤病毒等)的生產(chǎn)。ArcticZymesTechnologies成立于20世紀80年代后期,總部位于挪威北部的特羅姆瑟(Troms?)。立足北極海洋區(qū),致力于從海洋生物中識別新的冷適應(yīng)酶,用于分子研究、體外診斷和zhiliao領(lǐng)域。ArcticZymes專注于與全球的合作伙伴和商業(yè)創(chuàng)新者建立牢固可靠的關(guān)系。因此,我們一直在高水平工作,不斷滿足并且超過合作伙伴的期望。江西培養(yǎng)基條件中鹽核酸酶M-SAN HQ中鹽核酸酶更適合細胞基因drug(如AAV、LVV、RV及OV等)的生產(chǎn)。
逆轉(zhuǎn)錄病毒載體可以將7.5Kb左右外源基因整合入靶細胞基因組,并穩(wěn)定持久地表達,已經(jīng)在批準的CAR-T產(chǎn)品和許多臨床產(chǎn)品中得到應(yīng)用。Shou個成功的基因藥物臨床試驗是利用小鼠白血病病毒(Murin Leukemia Virus,MLV,gamma逆轉(zhuǎn)錄病毒)作為基因轉(zhuǎn)移載體醫(yī)治兒童的X性染色體連鎖嚴重聯(lián)合免疫缺陷(SCID-X1)。目前上市的6個細胞藥物產(chǎn)品全部采用逆轉(zhuǎn)錄病毒(3個為gamma逆轉(zhuǎn)錄病毒載體,3個慢病毒載體)作為基因轉(zhuǎn)移載體。逆轉(zhuǎn)錄病毒載體目前常用的主要有兩個:gamma逆轉(zhuǎn)錄病毒載體(Retroviral vector,RV)和慢病毒載體(Lentivirus vector,LV)。兩種病毒均屬于逆轉(zhuǎn)錄病毒科,在自身攜帶的逆轉(zhuǎn)錄酶催化下將其正鏈RNA均逆轉(zhuǎn)錄為cDNA。病毒顆粒比較大,約為100nm(70-100nm,有的至200nm),外層為表面突起的脂蛋白套膜,套膜內(nèi)為20面體的衣殼(capsid),核衣殼內(nèi)由一螺旋結(jié)構(gòu)的核酸。
除了獲得載體的滴度及產(chǎn)量,生產(chǎn)慢病毒更關(guān)心的指標主要是各種污染物的去除。總DNA污染的去除百分比在99.1-99.84%,總蛋白污染物的去除百分比在99.85-99.9%。針對宿主細胞的DNA(HCD)及蛋白(HCP),有報道其去除百分比分別為99.8%和99.4%。因為不僅殘存的DNA可能是個問題,而且DNA的大小以及由此引起的可能轉(zhuǎn)移整個有功能的開放閱讀框也是問題,因此監(jiān)管機構(gòu)對殘存DNA污染的分子量上限的要求越來越高。例如,F(xiàn)DA的指南‘生產(chǎn)用于傳染病適應(yīng)癥的病毒疫苗的細胞基質(zhì)和其他生物材料的特性和鑒定’中說明,殘留的細胞宿主的DNA片段不能超過一個功能基因的長度,估計在200bp左右。794398 徐州中鹽核酸酶價格哪家好呢,歡迎咨詢上海倍篤生物 。

慢病毒大規(guī)模純化的捕獲步驟包括:膜過濾澄清,隨后切向流過濾/超濾或者體積排阻色譜濃縮。此外,需用核酸酶(benzonase或M-SAN HQ中鹽核酸酶)來去除細胞殘留的、質(zhì)粒來源的DNA污染。這兩個步驟順序可以調(diào)整,依據(jù)項目工藝而定。兩種工藝路線各有優(yōu)缺點:先用核酸酶消化的優(yōu)點是可去除大的DNA片段,且后續(xù)步驟可以去除殘留核酸酶;但所用的核酸酶的量也非常大。與此相反,將核酸酶步驟后置的優(yōu)點是大幅降低核酸酶的量(成本降低);但后面的步驟必須有將核酸酶去除的能力。此外,后期用核酸酶的缺點是核酸污染可能會結(jié)合慢病毒顆粒形成沉淀,進而導(dǎo)致慢病毒在純化中流失,從而影響得率。相比傳統(tǒng)的全能核酸酶,M-SAN HQ中鹽核酸酶在生理鹽條件下,對HCD的去除效率更高。揚州70950-150中鹽核酸酶采購
中鹽核酸酶更適合細胞培養(yǎng)體系,相比全能核酸酶,酶用量減少到1/3-1/2,HCD去除效率更高。揚州70950-150中鹽核酸酶采購
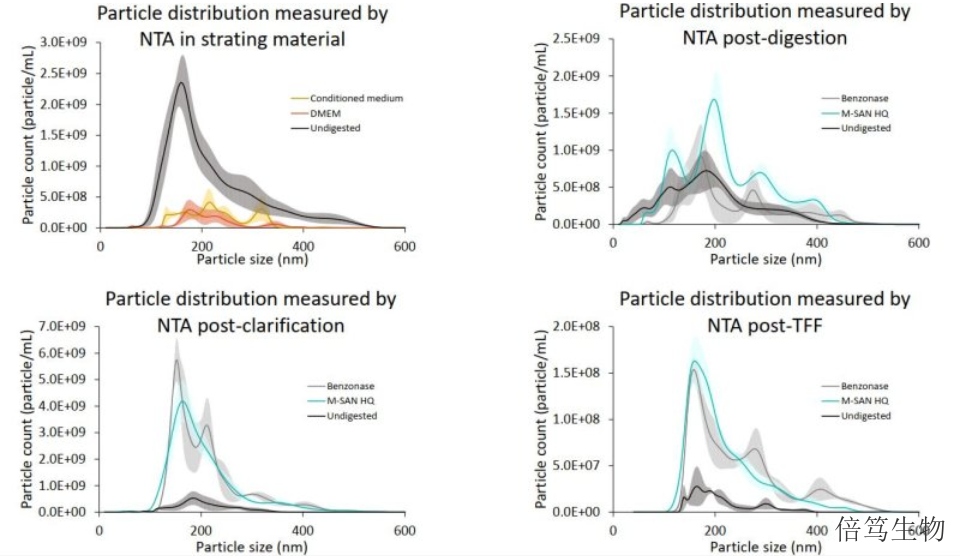
文章作者按照經(jīng)典的慢病毒載體生產(chǎn)流程操作,在融化、核酸酶消化、澄清、超濾等步驟留樣,分別檢測dsDNA濃度及功能性LV病毒滴度。經(jīng)過分析發(fā)現(xiàn),——去除主要發(fā)生在澄清環(huán)節(jié),能去除dsDNA的80%-90%;2. M-SAN HQ中鹽核酸酶比Benzonase能更高效去除dsDNA,即M-SAN HQ組的TFF回流液中dsDNA殘留量是Benzonase組回流液的20%左右;3. LV病毒滴度在澄清環(huán)節(jié)損失30%-40%;4. M-SAN HQ組的TFF回流液中LV病毒滴度略高于Benzonase組的回流液數(shù)據(jù)。揚州70950-150中鹽核酸酶采購
- 70950-202高鹽核酸酶價格表 2025-12-19
- 宣城SAN HQ高鹽核酸酶報價表 2025-12-19
- 上海貨號高鹽核酸酶廠家直銷 2025-12-19
- 重慶貨號高鹽核酸酶銷售電話 2025-12-19
- 安徽70950-202高鹽核酸酶 2025-12-19
- 天津哪里有高鹽核酸酶哪家公司銷售 2025-12-19
- 北京綜合高鹽核酸酶用途 2025-12-19
- 歷城區(qū)倍篤高鹽核酸酶供應(yīng)商 2025-12-19
- 連云港70921-160高鹽核酸酶銷售電話 2025-12-19
- 市中區(qū)倍篤高鹽核酸酶工廠直銷 2025-12-19
- 云南有什么助踝器銷售電話 2025-12-21
- 山東乳液藻油DHA原料應(yīng)用場景 2025-12-21
- 泡沫植絨拭子檢測 2025-12-21
- 洛陽可三甲聯(lián)動的醫(yī)護型老年護理中心地址 2025-12-21
- 虹口區(qū)運用實驗儀器服務(wù)費 2025-12-21
- 無外泌體培養(yǎng)基價格 2025-12-21
- 微機熔點儀定制 2025-12-21
- 金山區(qū)推薦吻合器工廠直銷 2025-12-21
- 青海哪里有金針招商加盟 2025-12-21
- 血漿外泌體提取報價 2025-12-21