細(xì)胞基因檢測科研服務(wù)
實(shí)驗(yàn)設(shè)計(jì)的合理性直接影響結(jié)果可信度。首先,細(xì)胞類型選擇需與研究目標(biāo)匹配,如腫瘤細(xì)胞系(HeLa、MCF-7)適用于抗ancer藥物篩選,原代細(xì)胞(如人臍靜脈內(nèi)皮細(xì)胞)則更貼近生理環(huán)境。其次,處理?xiàng)l件(如藥物濃度、作用時間)需通過預(yù)實(shí)驗(yàn)優(yōu)化,例如,某生長因子在10ng/mL濃度下促進(jìn)成纖維細(xì)胞增殖,但20ng/mL可能誘導(dǎo)分化而非增殖。對照設(shè)置至關(guān)重要,陽性對照(如含血清培養(yǎng)基)驗(yàn)證實(shí)驗(yàn)系統(tǒng)有效性,陰性對照(如無血清培養(yǎng)基)排除基礎(chǔ)增殖干擾,空白對照(無細(xì)胞)校正背景噪聲。此外,重復(fù)次數(shù)(通常≥3次)和隨機(jī)分組可減少誤差。例如,在篩選促進(jìn)角質(zhì)形成細(xì)胞增殖的中藥提取物時,通過正交實(shí)驗(yàn)設(shè)計(jì)優(yōu)化濃度與時間參數(shù),顯著提高了結(jié)果重復(fù)性。生物科研常借助 PCR 擴(kuò)增特定 DNA 的片段,用于檢測與分析。細(xì)胞基因檢測科研服務(wù)
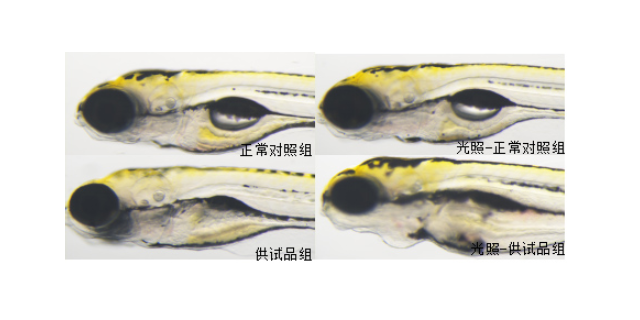
動物PDX模型的成功構(gòu)建依賴于三大技術(shù)突破。首先,tumor組織處理技術(shù)采用低溫保存液(4℃)配合短時間運(yùn)輸(<2小時),結(jié)合Matrigel基質(zhì)膠包裹,確保了腫瘤細(xì)胞的活性。例如,在結(jié)直腸ancerPDX模型構(gòu)建中,將患者手術(shù)標(biāo)本切成2-3mm3碎片,浸入含10%FBS的DMEM保存液,通過超聲引導(dǎo)原位植入小鼠盲腸壁,術(shù)后B超監(jiān)測顯示tumor血管生成模式與患者CT影像高度相似。其次,活的體成像技術(shù)的引入實(shí)現(xiàn)了動態(tài)追蹤——生物發(fā)光成像可檢測到直徑1mm的tumor,PET/CT則能量化tumor代謝活性。更關(guān)鍵的是,單細(xì)胞測序技術(shù)揭示了PDX模型中tumor微環(huán)境的動態(tài)變化:在乳腺ancerPDX模型中,移植后第2代tumor的免疫浸潤細(xì)胞比例(如Treg細(xì)胞)與患者原發(fā)灶差異小于15%,而傳統(tǒng)細(xì)胞系模型這一差異超過40%。這種“時空連續(xù)性”的保留,為研究tumor演化提供了獨(dú)特平臺。細(xì)胞增殖毒性科研服務(wù)生物科研中,生物統(tǒng)計(jì)學(xué)為實(shí)驗(yàn)設(shè)計(jì)與結(jié)果分析提供依據(jù)。

PDX原位模型的成功構(gòu)建依賴于三大技術(shù)突破。首先,免疫缺陷小鼠品系的迭代(如NSG、NOG小鼠)通過T/B/NK細(xì)胞三重缺陷設(shè)計(jì),將移植成功率從傳統(tǒng)裸鼠的不足10%提升至60%以上。其次,tumor組織預(yù)處理技術(shù)采用Matrigel基質(zhì)膠包裹tumor碎片,結(jié)合低溫保存液(4℃)2小時內(nèi)運(yùn)輸?shù)囊?guī)范,確保了腫瘤細(xì)胞的活性。例如,美迪西在構(gòu)建胃ancerPDX模型(如091Ga、122Ga)時,通過超聲引導(dǎo)原位植入技術(shù),將tumor塊精細(xì)定位至胃壁,術(shù)后B超監(jiān)測顯示tumor血管生成模式與患者CT影像高度相似。此外,活的體成像技術(shù)(如PET/CT、生物發(fā)光成像)的引入,實(shí)現(xiàn)了對tumor代謝、轉(zhuǎn)移過程的非侵入式追蹤,為藥效評價提供了動態(tài)數(shù)據(jù)支持。
促進(jìn)細(xì)胞增殖試驗(yàn)在基礎(chǔ)研究和臨床應(yīng)用中均發(fā)揮關(guān)鍵作用。在基礎(chǔ)研究領(lǐng)域,該試驗(yàn)揭示了Wnt/β-catenin信號通路對腸上皮干細(xì)胞增殖的調(diào)控機(jī)制,為結(jié)直腸ancer醫(yī)療提供新靶點(diǎn)。在臨床轉(zhuǎn)化方面,重組人表皮生長因子(rhEGF)凝膠通過促進(jìn)角質(zhì)形成細(xì)胞增殖,加速燒傷創(chuàng)面愈合,已獲批用于臨床。近年來,技術(shù)進(jìn)步推動了試驗(yàn)升級,如高內(nèi)涵篩選系統(tǒng)結(jié)合熒光標(biāo)記,可同時檢測細(xì)胞增殖、遷移和凋亡;類organ模型與微流控芯片的整合,模擬體內(nèi)復(fù)雜環(huán)境,提高結(jié)果臨床相關(guān)性。例如,利用患者來源tumor類organ篩選促進(jìn)T細(xì)胞增殖的免疫檢查點(diǎn)抑制劑,明顯提升了個性化醫(yī)療成功率。未來,隨著單細(xì)胞測序和AI分析技術(shù)的融入,該試驗(yàn)將在精細(xì)醫(yī)療和再生醫(yī)學(xué)中發(fā)揮更大價值。藥物研發(fā)在生物科研中歷經(jīng)多階段,確保藥物有效性。
動物PDX模型(Patient-DerivedTumorXenograft)通過將患者tumor組織直接移植至免疫缺陷動物體內(nèi),構(gòu)建出高度模擬人體tumor微環(huán)境的“活的體復(fù)刻系統(tǒng)”。與傳統(tǒng)細(xì)胞系移植不同,PDX模型保留了tumor組織的原始異質(zhì)性,包括ancer細(xì)胞亞群、間質(zhì)細(xì)胞比例及血管生成模式。例如,在非小細(xì)胞肺ancerPDX模型中,移植的tumor組織可復(fù)現(xiàn)患者原發(fā)灶中70%-90%的基因突變譜,且對化療藥物的響應(yīng)率與臨床結(jié)果相關(guān)性達(dá)82%。免疫缺陷動物的選擇是關(guān)鍵——NOD/SCID小鼠因缺乏T、B細(xì)胞且NK細(xì)胞活性低,成為早期主流宿主;而新一代NSG(NOD-scidIL2Rγnull)小鼠通過敲除IL-2受體γ鏈進(jìn)一步抑制NK細(xì)胞,使移植成功率從40%提升至65%以上。這種“原汁原味”的tumor保留能力,使PDX模型成為連接基礎(chǔ)研究與臨床轉(zhuǎn)化的關(guān)鍵工具。生物科研的胚胎發(fā)育研究揭示生命起始奧秘。中性粒細(xì)胞遷移實(shí)驗(yàn)費(fèi)用
干細(xì)胞研究是生物科研熱點(diǎn),為再生醫(yī)學(xué)帶來無限希望。細(xì)胞基因檢測科研服務(wù)
CDX 模型培訓(xùn)在倫理與法規(guī)方面也有相應(yīng)的教育環(huán)節(jié)。學(xué)員要了解在使用實(shí)驗(yàn)動物構(gòu)建 CDX 模型過程中必須遵循的倫理原則和相關(guān)法規(guī)要求。例如,要確保動物實(shí)驗(yàn)的必要性、減少動物的痛苦和不適、采用人道的實(shí)驗(yàn)方法等。培訓(xùn)將詳細(xì)講解實(shí)驗(yàn)動物使用許可證的申請流程、動物實(shí)驗(yàn)方案的倫理審查程序等內(nèi)容,使學(xué)員樹立正確的動物實(shí)驗(yàn)倫理觀念,在進(jìn)行 CDX 模型研究時嚴(yán)格遵守法律法規(guī),保障動物福利的同時也確保研究的合法性和可持續(xù)性,避免因違反倫理法規(guī)而導(dǎo)致的研究中斷或不良后果。細(xì)胞基因檢測科研服務(wù)
- 福建斑馬魚實(shí)驗(yàn)文獻(xiàn) 2025-12-19
- 貴州斑馬魚實(shí)驗(yàn) 2025-12-19
- 天津斑馬魚實(shí)驗(yàn)基因突變 2025-12-19
- 斑馬魚暴露毒性試驗(yàn) 2025-12-19
- 斑馬魚養(yǎng)殖費(fèi)用 2025-12-19
- 山西斑馬魚實(shí)驗(yàn)化妝品 2025-12-19
- 浙江免疫藥物臨床前評價 2025-12-18
- 浙江生物醫(yī)藥臨床前cro公司 2025-12-18
- 浙江nmpa臨床前安全性評估 2025-12-18
- 遺傳毒性評價實(shí)驗(yàn)在新藥臨床前 2025-12-18
- 長寧區(qū)品牌裝卸搬運(yùn)好處 2025-12-19
- 中山工業(yè)制造erp系統(tǒng)教程 2025-12-19
- 太倉抖音運(yùn)營答疑解惑 2025-12-19
- 靜安區(qū)第三方會議及展覽服務(wù)介紹 2025-12-19
- 杭州疑難核名服務(wù)代理記賬條件 2025-12-19
- 珠海重型設(shè)備物流服務(wù)方案 2025-12-19
- 青少年糾正教育 2025-12-19
- 斯里蘭卡紡織展會參展須知 2025-12-19
- 長寧區(qū)企業(yè)形象策劃費(fèi)用 2025-12-19
- 寶山區(qū)一站式保潔服務(wù)服務(wù)電話 2025-12-19