新藥藥理學實驗
心血管藥物在維護人類心臟健康方面發揮著關鍵作用。例如他汀類藥物,是臨床上常用的降脂藥,通過抑制膽固醇合成過程中的關鍵酶,降低血液中低密度脂蛋白膽固醇(LDL-C)的水平。高 LDL-C 水平是動脈的粥樣硬化的重要危險因素,他汀類藥物的應用可以有效減少動脈的粥樣硬化斑塊的形成,降低guanxin病、心肌梗死等心血管疾病的發病風險。此外,抗高的血壓藥物種類繁多,如血管緊張素轉換酶抑制劑(ACEI),它通過抑制血管緊張素轉換酶的活性,減少血管緊張素 II 的生成,從而舒張血管,降低人體血壓。這些心血管藥物的合理使用需要醫生根據患者的具體病情,如血壓、血脂水平、是否合并其他疾病等綜合考慮,制定個性化的治療方案,并且患者需要長期規律服藥,同時配合健康的生活方式,如低鹽低脂飲食、適量運動等,才能更好地控制心血管疾病的發展。利用斑馬魚模型評價骨質疏松癥。新藥藥理學實驗
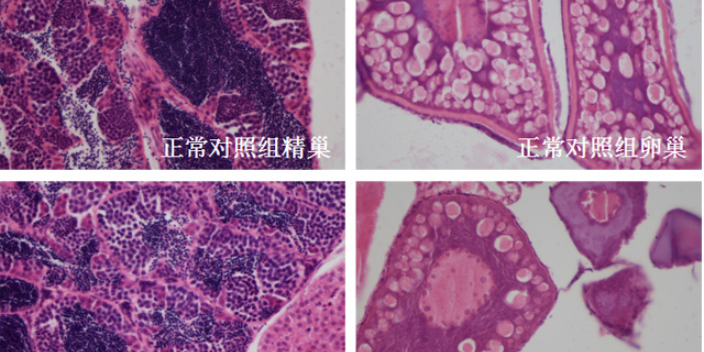
中藥藥效評價需結合體內外實驗模型,驗證其醫療作用。體外實驗常用細胞模型,如人肝ancer細胞HepG2用于評估中藥抗tumor活性。例如,研究發現黃連素可通過誘導細胞凋亡抑制肝ancer細胞增殖。體內實驗則依賴動物模型,如糖尿病小鼠模型用于測試中藥降糖效果。例如,六味地黃丸可明顯降低糖尿病小鼠的空腹血糖和糖化血紅蛋白水平。此外,網絡藥理學技術通過整合多組學數據,預測中藥與靶點的相互作用,為實驗設計提供方向。例如,通過構建“成分-靶點-疾病”網絡,發現黃芪多糖可能通過調節PI3K/Akt信號通路發揮免疫調節作用。藥物安全性及有效性評價研究斑馬魚模型評價腎臟毒性。
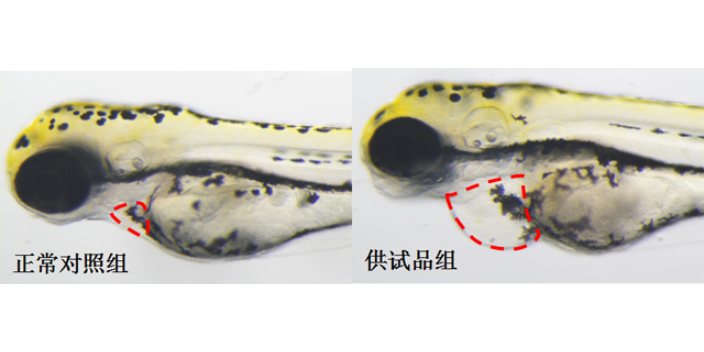
隨著電子產品的大量使用,用眼的時間和強度已遠超過去,用眼過度引起一系列視力問題。研究表明,高度近視、視網膜疾病、白內障、眼干燥關節綜合征均與眼細胞凋亡相關。斑馬魚的眼部血管結構跟人非常相似,斑馬魚視網膜結構也跟人高度相似。用霉酚酸嗎啉乙酯可以誘發斑馬魚眼細胞凋亡,模擬人的眼部疾病。用特異性熒光染色(呈綠色),患有眼疾的斑馬魚眼細胞凋亡較正常斑馬魚明顯增多,在熒光顯微鏡下可以觀察到。我們將受測試斑馬魚分成三組,分別是正常對照組、模型對照組和藥物組。其中正常對照組未攝入霉酚酸嗎啉乙酯,模型對照組與服用眼保護劑組都攝入了等量的霉酚酸嗎啉乙酯(霉酚酸嗎啉乙酯通過溶解到養魚用水中的方式攝入到斑馬魚體內)。眼保護劑組在攝入霉酚酸嗎啉乙酯的同時攝入藍莓葉黃素酯之類的眼保護劑。服用一段時間眼保護劑后,我們對斑馬魚整體做凋亡細胞特異性染色,觀察細胞凋亡,同時制作成病理切片觀察眼部的病理結構變化。
基于斑馬魚模型實驗,可進行活性化合物發現、高通量藥物篩選、藥效評價、安全性評價、生物學質量控制等臨床前研究,實驗周期短、成本低,結果直觀,助力醫藥企業的藥物研發、品控及宣傳推廣。利用斑馬魚模型評價氧化應激。斑馬魚的基因與人類基因的相似度達到87%,與哺乳動物對外源化學物質的防御機制相當,包括酶的誘導和氧化應激。當生物暴露在環境污染物中,生物可能會發生氧化應激,主要表現為活性氧(ROS)產生和消耗的不平衡。在需氧生物的活細胞中,活性氧被一種由水和脂溶性低分子量自由基清除劑、特異性抗氧化酶組成的抗氧化防御機制解。應用ROS特異性熒光檢測試劑,它的水解產物能被ROS氧化為高熒光物質,用多功能酶標儀檢測熒光值反映氧化應激的程度。本方法已被授予國家發明專利。利用斑馬魚模型評價糖尿病神經炎癥消退功效。

表觀遺傳調控,如DNA甲基化,通過干擾脂質代謝在人類肥胖發展中發揮作用。我們假設TBPH破壞代謝處理器,通過PPAR信號導致脂質穩態受損通路;然而,TBPH對脂質代謝的生物學作用仍有待闡明。據報道,許多環境污染物會破壞動物體內的脂質穩態,導致異常的脂質積累,主要是肝細胞中甘油三酯(TG)的積累,并伴隨肝細胞膨脹、炎癥和氧化應激。這些不良反應可能導致肝脂肪變性或從單純性脂肪肝轉變為代謝綜合征的肝臟表現,如非酒精性脂肪性肝病(NAFLD)的組織學表型。斑馬魚評價胃腸道粘膜損傷輔助保護功效。生物藥安評機構
利用斑馬魚模型評價抗焦慮功效。新藥藥理學實驗
在藥物開發的過程中,藥物的有效性評價是決定藥物終能否上市的關鍵之一。藥物有效性研究包括了動物試驗中的藥效學研究和人體臨床試驗中的有效性研究。對于藥物研發來說,動物藥效學試驗是人體試驗的基礎,因為如果一個化合物要作為藥物用于人類,必須要有一定的動物研究的結果,再用于人體研究,才符合倫理學的原則。因此動物研究的目的就是為保證化合物初次用于人體的安全有效性,動物試驗應顯示主要的藥效作用和毒性以及藥代動力學特性,人們需要根據動物試驗的結果為臨床試驗推薦適應癥、計算進入人體試驗的安全劑量。而只有通過人體臨床試驗證明藥物的安全有效性后,藥物才能終獲得上市,廣泛應用。新藥藥理學實驗
- 天津斑馬魚實驗基因突變 2025-12-19
- 浙江免疫藥物臨床前評價 2025-12-18
- 浙江生物醫藥臨床前cro公司 2025-12-18
- 浙江nmpa臨床前安全性評估 2025-12-18
- 遺傳毒性評價實驗在新藥臨床前 2025-12-18
- 浙江天然藥物臨床前前新藥評價中心 2025-12-18
- 云南小分子臨床前模式動物 2025-12-18
- 藥品臨床前 2025-12-18
- 深圳小分子臨床前安評實驗 2025-12-18
- 寧波藥物臨床前研究項目 2025-12-18
- 鶴壁工廠規劃方法論 2025-12-19
- 全方面GEO生成式引擎優化答疑解惑 2025-12-19
- 泉州自動化互聯網推廣推廣 2025-12-19
- 嘉定區本地市場營銷策劃五星服務 2025-12-19
- 崇明區電話智力游戲開發聯系方式 2025-12-19
- 河南拖車銷售 2025-12-19
- 河南主題廣告畫面印刷設計 2025-12-19
- 蘇州上門專利轉讓哪個好 2025-12-19
- 鹽田區人工智能專利申請答復 2025-12-19
- 六合區PTI試驗粉塵有哪些 2025-12-19